医疗器械工程师管理系统:如何实现高效协同与合规管理
在医疗科技快速发展的今天,医疗器械工程师作为产品设计、研发、测试和质量保障的核心力量,其工作流程的规范化、信息化和可追溯性变得尤为重要。一个科学高效的医疗器械工程师管理系统(Medical Device Engineer Management System, MDEMS)不仅是企业提升研发效率的关键工具,更是满足法规合规(如ISO 13485、FDA 21 CFR Part 820、中国NMPA要求)的重要支撑。
一、为什么要建立医疗器械工程师管理系统?
传统的人工管理方式存在诸多痛点:任务分配不透明、进度跟踪困难、文档版本混乱、人员技能难以匹配项目需求、知识沉淀缺失等。这些问题不仅影响项目交付周期,还可能因不符合监管要求而导致产品召回或法律风险。
医疗器械行业具有高技术门槛、强法规约束和长生命周期等特点,对工程师的专业能力、责任意识和过程控制提出了更高要求。因此,建立一套覆盖“人-事-物-法”全链条的管理系统,已成为企业数字化转型的必选项。
二、系统核心功能模块设计
1. 工程师档案与能力画像
系统应建立每位工程师的电子档案,包括教育背景、专业认证(如注册医疗器械工程师)、项目经验、技能标签(如嵌入式开发、生物材料、电磁兼容等)。通过AI辅助打标与历史数据挖掘,形成动态的能力画像,便于精准匹配岗位需求与项目分工。
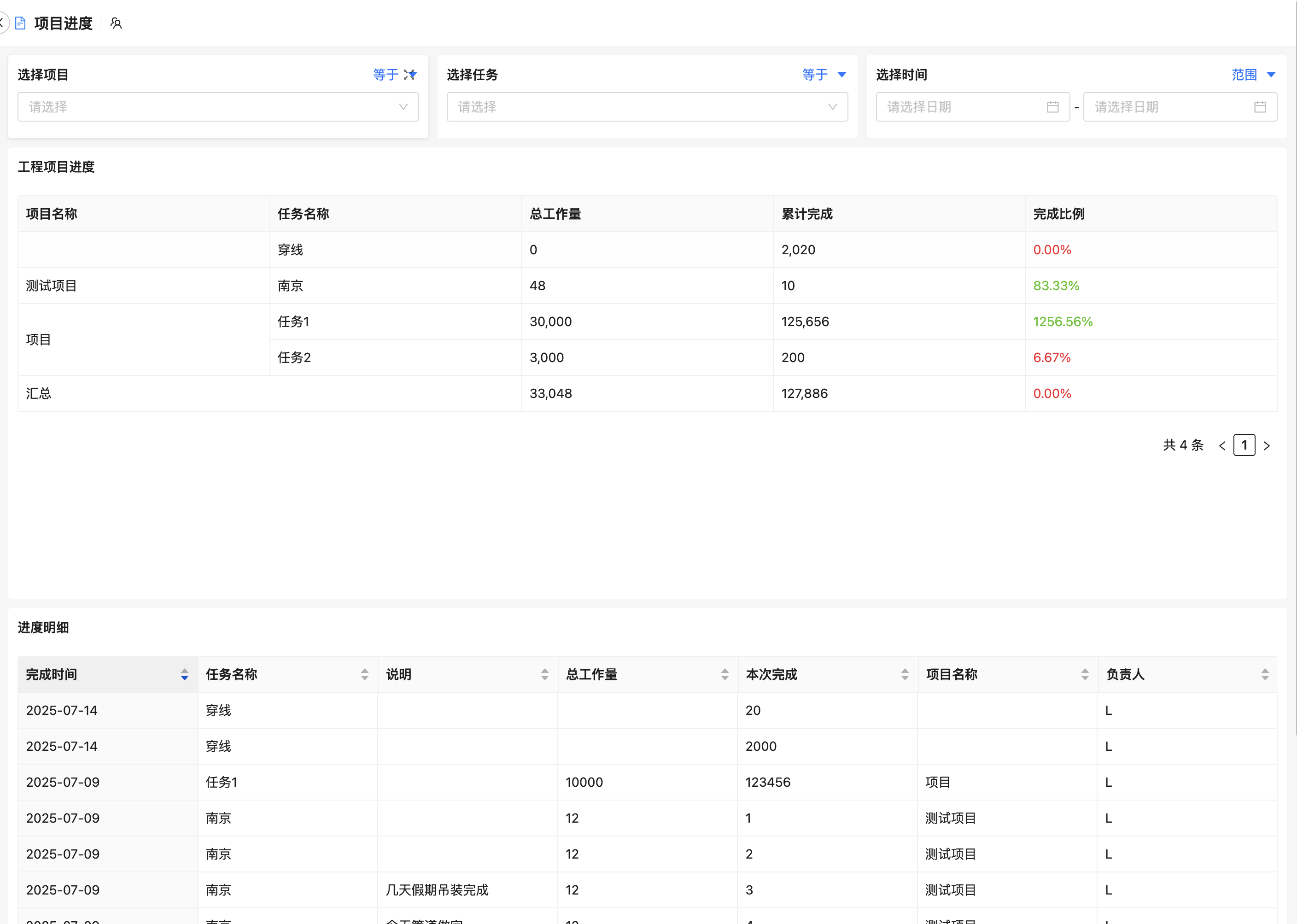
2. 项目任务与进度管理
集成敏捷开发理念(Scrum/Kanban),支持按阶段划分任务(概念设计→原型验证→临床前测试→注册申报),设置里程碑节点,并自动提醒关键路径延误。同时,与PLM(产品生命周期管理)系统打通,确保设计变更可追溯。
3. 文档与合规管理
所有设计文件、测试报告、风险分析文档均需上传至中央数据库,采用版本控制机制(Git-like结构),防止误操作导致的数据丢失。系统内置合规检查清单,例如:是否完成DFMEA、是否进行设计验证记录、是否有变更审批流程等,实时提示未达标项。
4. 资源调度与协作平台
整合实验室设备预约、样机使用登记、跨部门协作沟通等功能,避免资源冲突。支持在线评审会议纪要自动生成、问题闭环跟踪,提高团队协作效率。
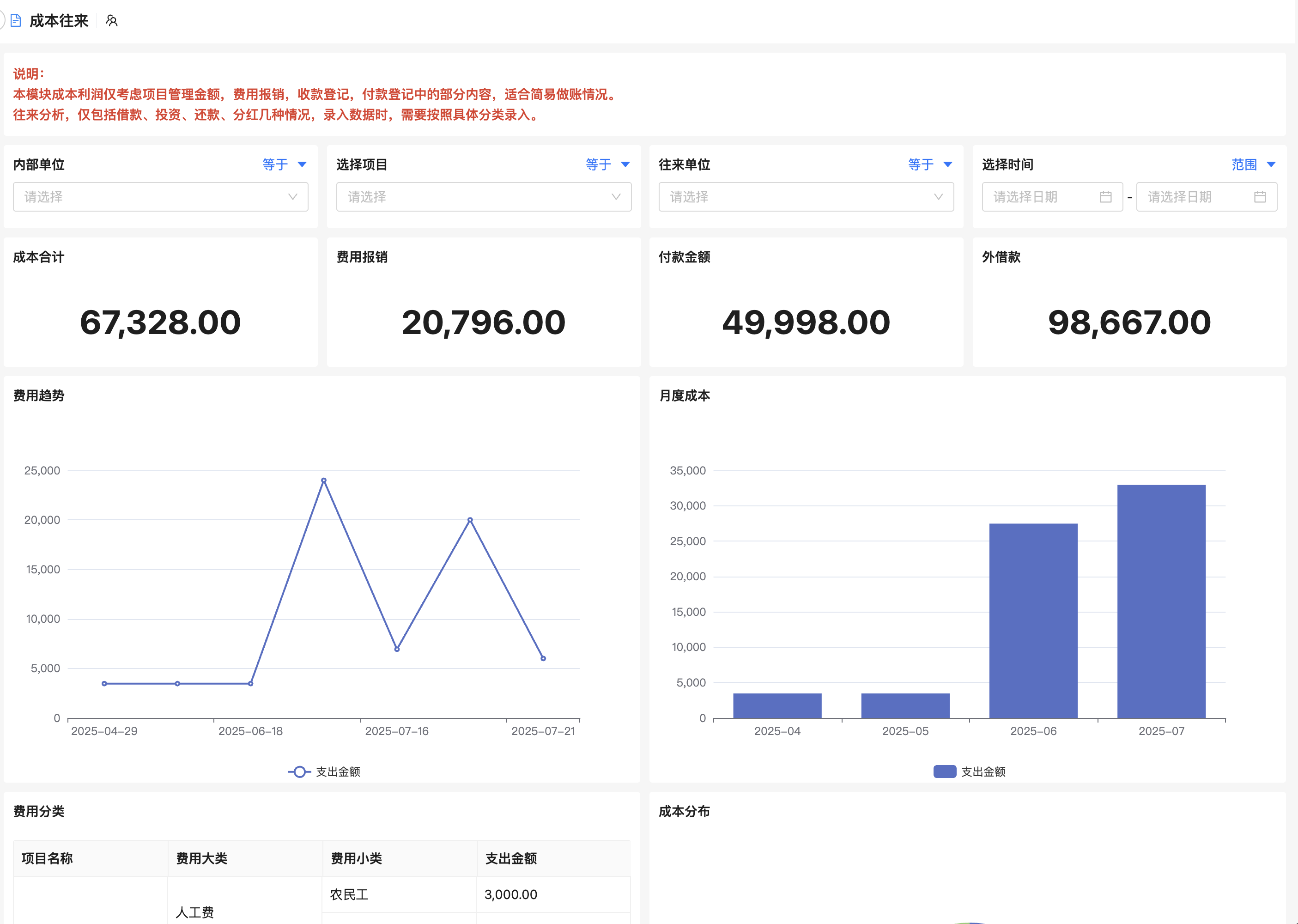
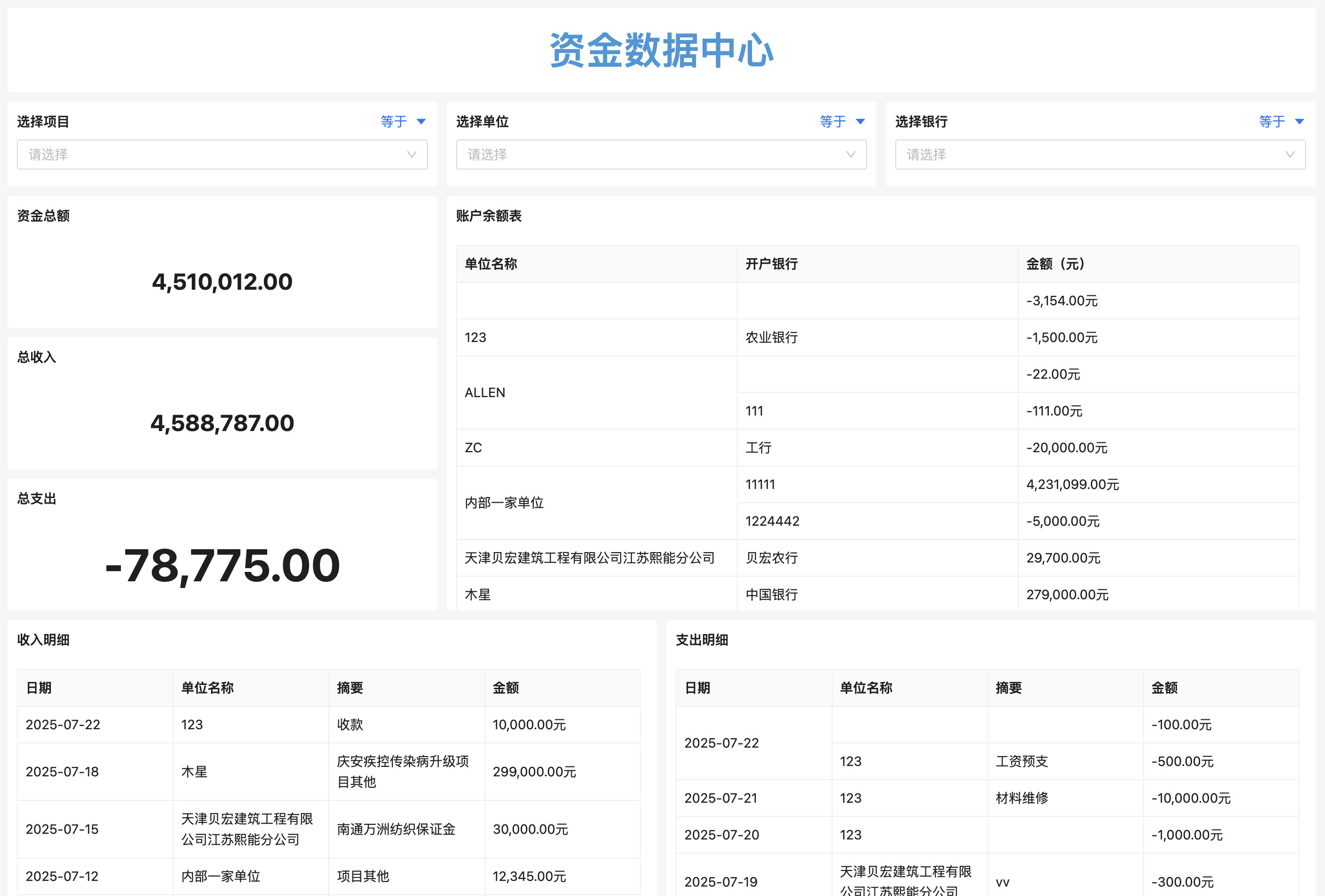
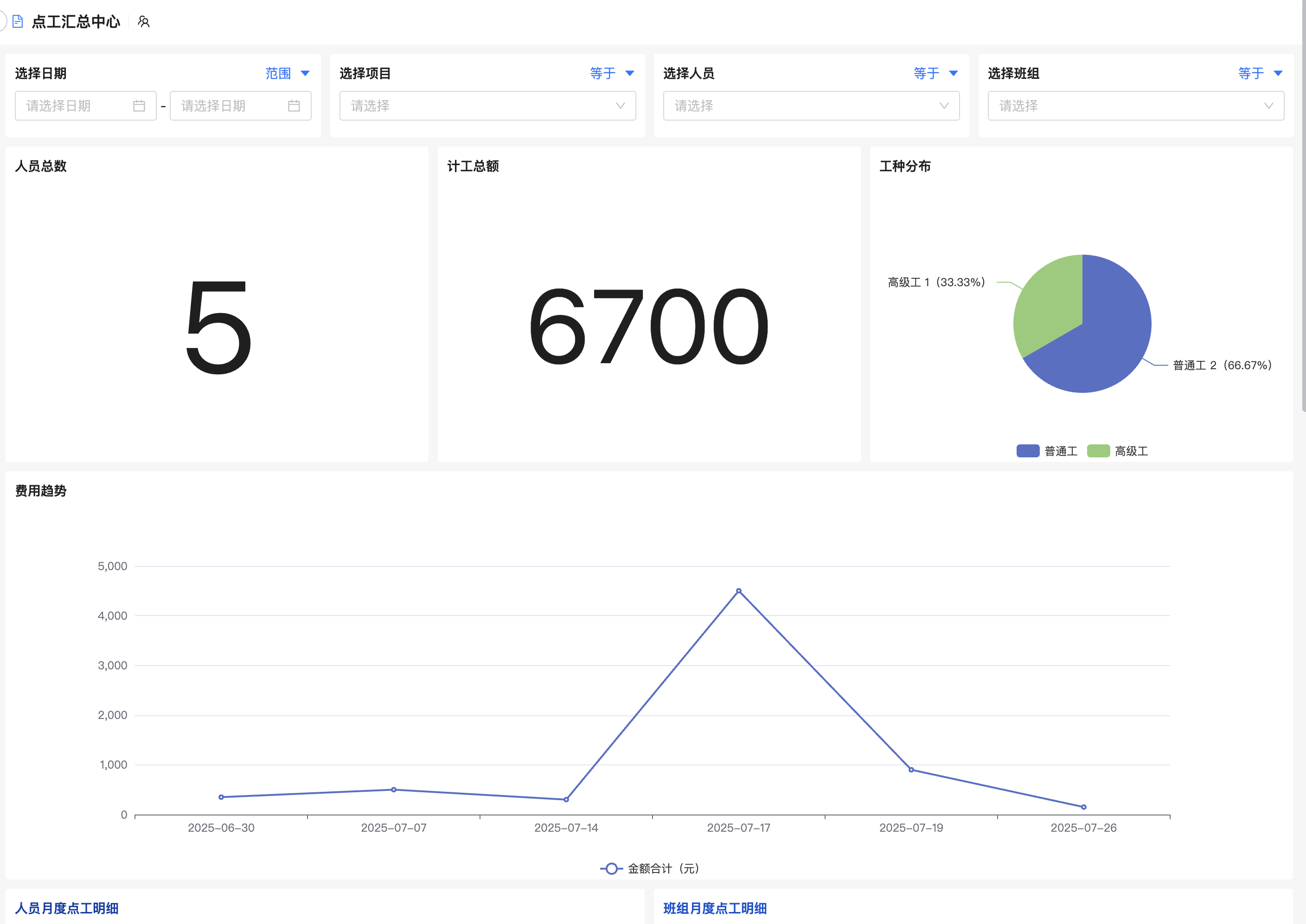
5. 数据分析与绩效评估
基于BI看板展示工程师产出率、缺陷密度、任务完成率等指标,结合KPI考核体系,为晋升、培训提供数据依据。同时,通过热力图分析项目瓶颈环节,优化资源配置。
三、关键技术实现路径
1. 微服务架构与云原生部署
采用Spring Boot + Docker + Kubernetes构建微服务架构,确保系统弹性扩展与高可用性。部署于私有云或混合云环境,保障敏感数据不出内网。
2. 权限分级与审计日志
严格遵循最小权限原则(Least Privilege),区分管理员、项目经理、工程师三级角色。每一步操作留痕,生成完整的审计日志,满足FDA 21 CFR Part 11电子签名要求。
3. API接口开放与生态集成
预留标准RESTful API供第三方系统接入,如ERP(采购)、MES(制造)、QMS(质量管理)等,打造统一数字化工厂生态。
4. 移动端适配与远程办公支持
开发响应式Web界面及移动端App,支持工程师随时随地查看任务、提交进度、拍照上传现场记录,适应灵活办公趋势。
四、实施步骤与成功案例参考
1. 需求调研与蓝图规划(1-2个月)
组织跨职能团队(研发、质量、IT、人事)访谈,梳理当前痛点与改进目标,制定分阶段上线计划。
2. 核心模块试点运行(3-6个月)
选择1-2个典型项目先行试用,收集反馈并迭代优化。重点关注用户接受度、流程适配性和数据准确性。
3. 全面推广与持续运营(6个月以上)
逐步覆盖全部工程师和项目,建立运维团队负责日常维护、权限更新、数据备份。定期举办“系统使用之星”评选,激励员工积极参与。
典型案例:某国产高端影像设备公司
该公司引入MDEMS后,平均项目交付周期缩短25%,文档错误率下降40%,首次通过FDA审核的概率提升至95%。更重要的是,新入职工程师可在一周内快速上手项目,显著降低培养成本。
五、常见误区与规避建议
- 误区一:只做流程自动化,忽视文化建设 —— 系统只是工具,真正价值在于改变思维习惯。应配套培训、奖惩机制推动文化落地。
- 误区二:过度定制化导致后期维护难 —— 建议优先选用成熟框架+少量二次开发,避免陷入“定制陷阱”。
- 误区三:忽略数据治理与安全合规 —— 必须提前设计数据分类分级策略,符合GDPR、网络安全法等要求。
六、未来发展趋势展望
随着AI大模型、低代码平台、数字孪生等新技术的发展,未来的医疗器械工程师管理系统将更加智能化:
- AI辅助设计建议(基于历史成功案例推荐最优方案)
- 语音输入自动生成会议纪要与任务派发
- 虚拟现实(VR)模拟测试场景,减少实物样机消耗
- 区块链存证关键文档,增强可信度与防篡改能力
总之,医疗器械工程师管理系统不是简单的软件替换,而是企业从“经验驱动”向“数据驱动”跃迁的战略举措。它既是工程效能的放大器,也是合规底线的守护者。对于正在迈向国际化、高质量发展的医疗器械企业而言,现在正是投资这一系统的最佳时机。