医药研发项目管理软件如何助力高效推进新药开发流程
在当今快速发展的医药行业中,新药研发周期长、成本高、风险大,传统的项目管理方式已难以满足复杂多变的研发需求。医药研发项目管理软件应运而生,成为连接科学家、项目经理、法规专家与财务团队的数字化中枢。它不仅优化了任务分配与进度跟踪,还通过数据驱动决策和合规性支持,显著提升研发效率与成功率。
为什么需要医药研发项目管理软件?
医药研发涉及多个阶段:靶点发现、先导化合物筛选、临床前研究、临床试验(I-IV期)、注册申报及上市后监测。每个阶段都需跨部门协作、大量数据记录与严格合规控制。若使用Excel表格或纸质文档进行管理,极易出现信息滞后、版本混乱、资源浪费等问题。
根据《Nature Reviews Drug Discovery》统计,全球平均一款新药从实验室到市场耗时约10–15年,成本超20亿美元。其中约30%的时间浪费在非科研活动上——如会议协调、数据整理、报告撰写等。医药研发项目管理软件正是解决这一痛点的关键工具。
核心功能模块解析
1. 项目规划与任务分解(WBS)
软件可基于标准研发流程(如ICH指南)自动生成工作分解结构(Work Breakdown Structure),将大型项目拆解为可执行的小任务,并分配责任人、截止日期和优先级。例如,在临床试验阶段,系统能自动划分“伦理审批”、“研究中心招募”、“患者入组”、“数据收集”等子任务,确保无遗漏。
2. 资源调度与预算控制
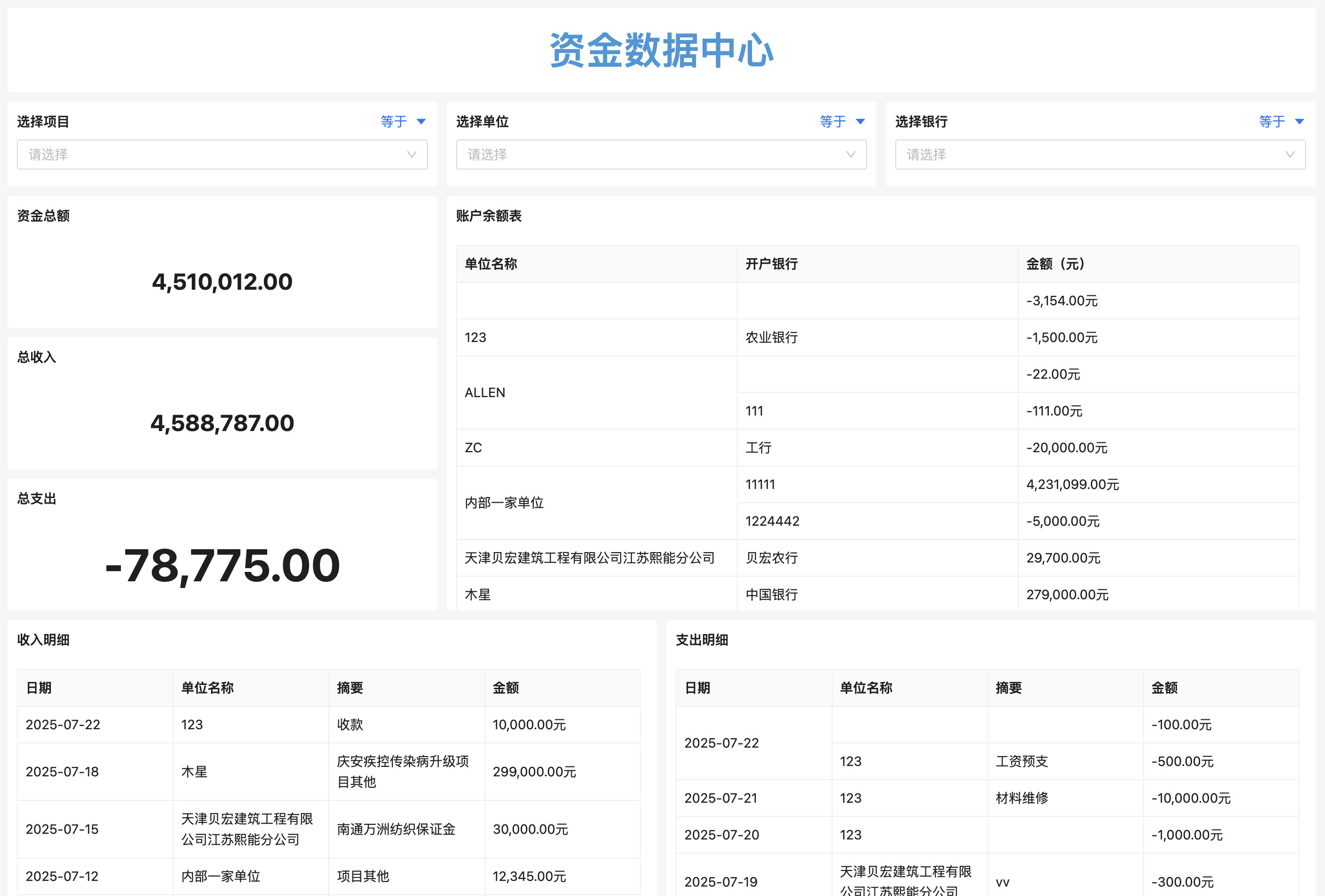
集成资源池功能,实时显示人员、设备、实验室空间等可用情况。项目经理可通过甘特图直观查看资源冲突并提前调整。同时,预算模块可绑定费用类型(人力、外包、材料),实现成本透明化,避免超支。某跨国药企曾通过该功能节省年均研发支出约8%。
3. 数据集中管理与合规审计
所有实验数据、文档、影像资料均可上传至中央数据库,按权限分级访问。内置电子签名、操作日志、版本历史等功能,完全符合FDA 21 CFR Part 11和EU Annex 15等法规要求,极大降低合规风险。
4. 实时进度监控与预警机制
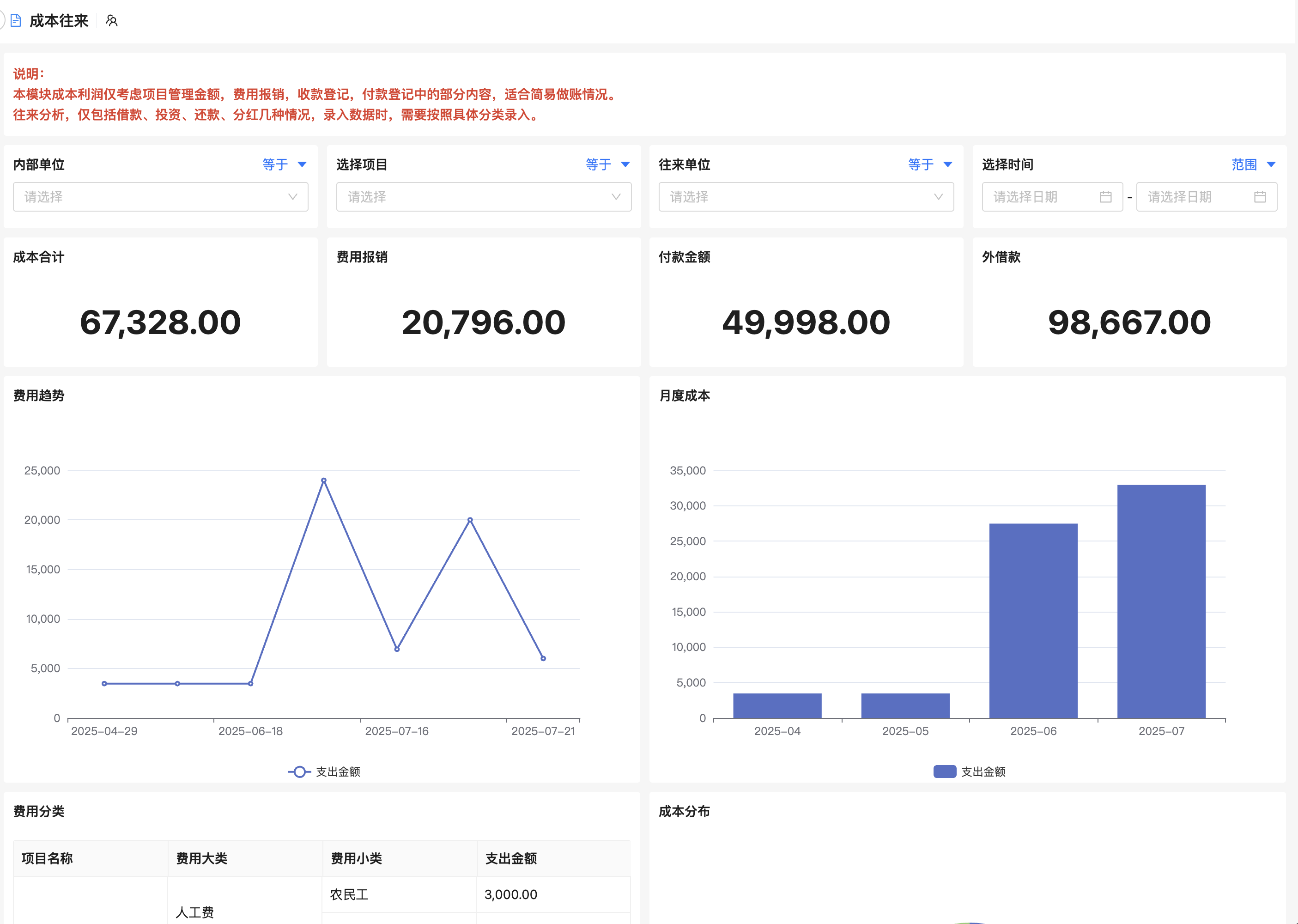
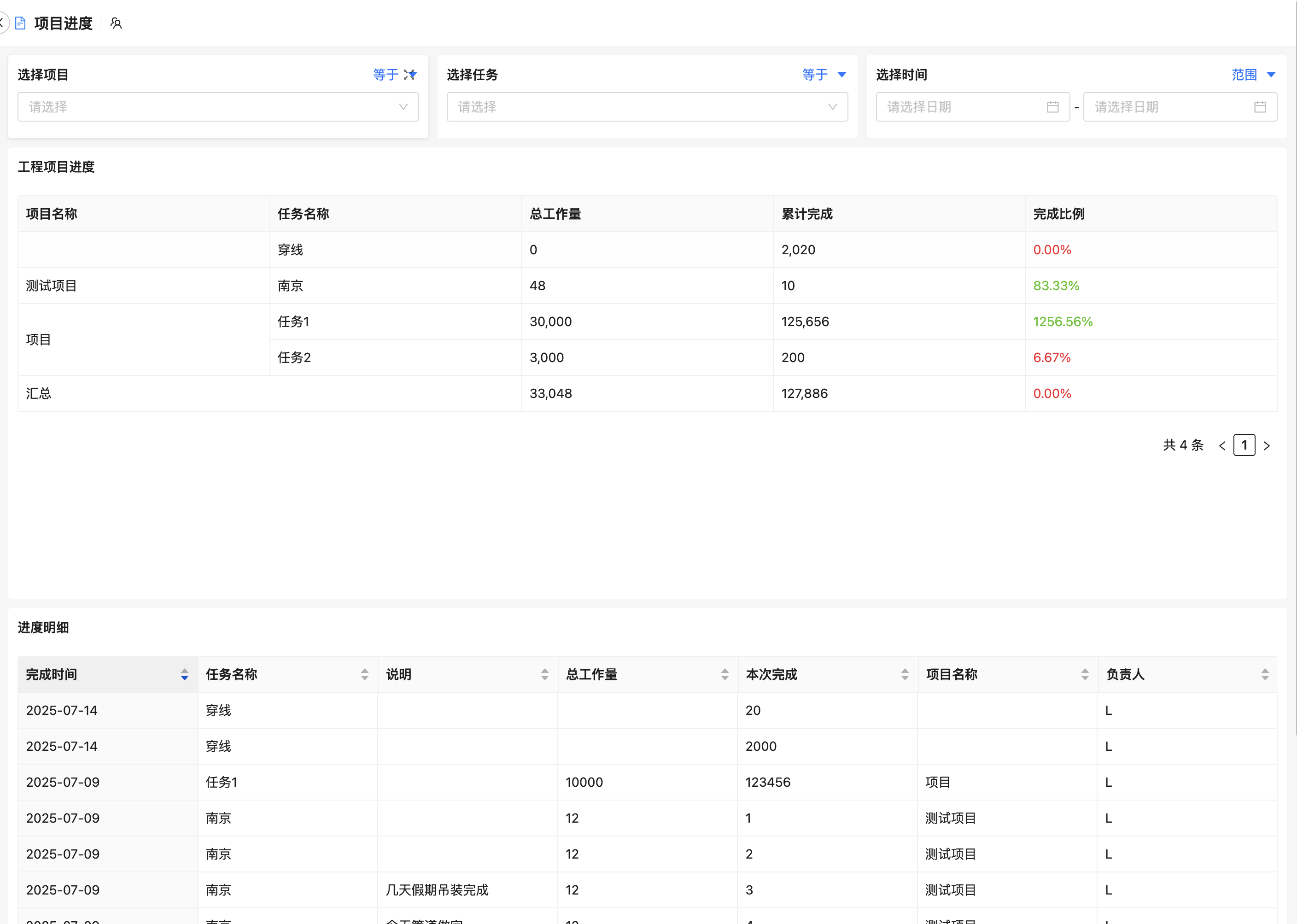
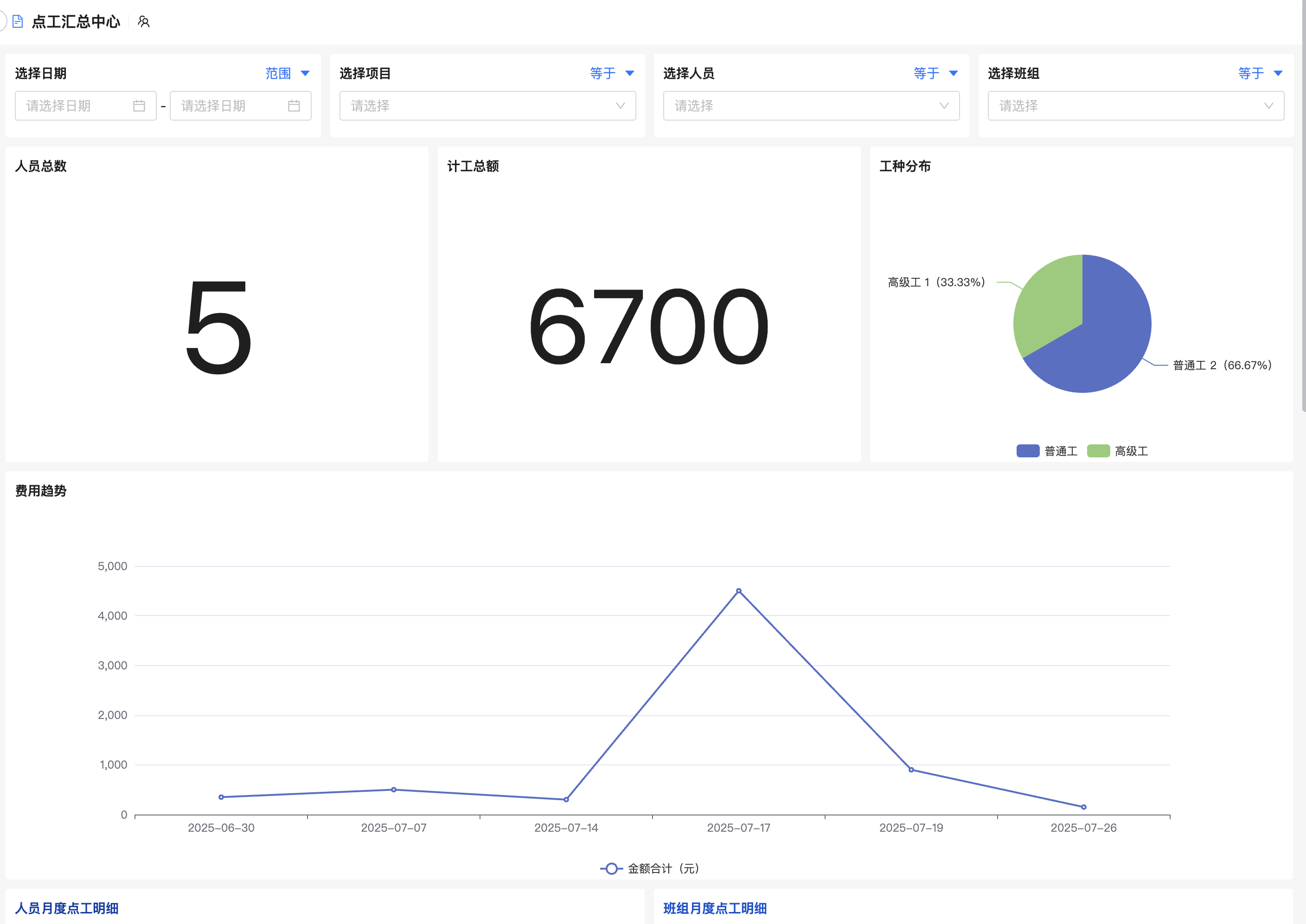
通过仪表盘展示关键绩效指标(KPI),如项目完成率、延期次数、偏差发生率。一旦某个环节延迟超过阈值(如临床试验入组慢于预期),系统会自动触发邮件或短信提醒相关负责人,促使问题早发现、早干预。
5. 集成AI辅助分析能力
部分先进平台已嵌入AI引擎,可对历史项目数据进行挖掘,预测潜在瓶颈(如某研究中心过去三次试验均因招募困难延期)。还能结合外部数据库(如ClinicalTrials.gov)推荐合适的合作机构或试验方案。
实施建议:从选型到落地
第一步:明确业务需求
不同企业规模和研发方向差异巨大。初创生物技术公司可能更关注敏捷开发与成本控制,而大型制药集团则侧重多中心协同与全球合规。因此,必须先梳理当前痛点:是数据分散?进度不透明?还是合规压力大?这决定了后续软件的功能选择。
第二步:评估供应商与平台成熟度
市面上主流产品包括Veeva Vault、SAP Clinical Development、IBM Watson Health、以及国产的数智云、启明医药等。评估时重点关注:是否支持私有化部署?API开放程度?是否有行业成功案例?能否对接现有ERP或LIMS系统?例如,Veeva在欧美市场占有率高,但本地化服务较弱;国产软件响应快、定制灵活,适合快速迭代场景。
第三步:分阶段上线与培训
切忌一次性全量切换。建议先在一个项目组试点运行3–6个月,收集反馈后再逐步推广至全公司。同时,开展分角色培训(科研人员、项目经理、QA专员)至关重要,确保用户熟练掌握操作逻辑,减少抵触情绪。
第四步:建立持续优化机制
软件上线不是终点,而是起点。定期召开“数字化复盘会”,分析哪些功能使用频率低、哪些流程仍存在卡点,持续优化配置。还可引入第三方咨询机构做年度健康检查,保持系统始终贴合业务发展。
未来趋势:向智能化与生态化演进
未来的医药研发项目管理软件将不再只是“记事本”,而是具备更强的智能决策能力:
- 预测性分析:利用机器学习模型预测项目失败概率,帮助管理层提前干预。
- 区块链溯源:保障临床试验数据不可篡改,增强监管信任。
- 云原生架构:支持弹性扩容,适应突发性大规模试验需求。
- 跨组织协作平台:打通CRO、医院、监管机构之间的壁垒,构建开放创新生态。
例如,辉瑞与IBM合作开发的AI驱动平台,已在新冠疫苗研发中实现了从靶点识别到临床设计的全流程自动化,缩短时间近40%。
结语:数字化转型不是选择题,而是必答题
面对日益激烈的市场竞争和不断升级的监管要求,医药企业唯有拥抱数字化工具,才能在新药研发这场马拉松中赢得先机。医药研发项目管理软件不仅是效率工具,更是战略资产——它让科学更有条理,让创新更有保障,让每一分投入都能转化为实实在在的患者价值。